Чистые вещества и смеси. Способы разделения смесей
В нашей статье мы рассмотрим, что такое чистые вещества и смеси, способы разделения смесей. В повседневной жизни их использует каждый из нас. А встречаются ли вообще в природе чистые вещества? И как отличить их от смесей?
Чистые вещества и смеси: способы разделения смесей
Чистыми называют вещества, которые содержат частицы только определенного вида. Ученые считают, что в природе их практически не существует, поскольку все они, хоть и в ничтожных долях, содержат примеси. Абсолютно все вещества также являются растворимыми в воде. Даже если погрузить в эту жидкость, к примеру, серебряное кольцо, ионы этого металла перейдут в раствор.
Признаком чистых веществ являются постоянство состава и физических свойств. В процессе их образования происходит изменение количества энергии. Причем она может как увеличиваться, так и уменьшаться. Разделить чистое вещество на отдельные составляющие можно только с помощью химической реакции. К примеру, только дисциллированная вода обладает типичной для этого вещества температурой кипения и замерзания, отсутствием вкуса и запаха. А разложить ее кислород и водород можно только путем электролиза.
К примеру, только дисциллированная вода обладает типичной для этого вещества температурой кипения и замерзания, отсутствием вкуса и запаха. А разложить ее кислород и водород можно только путем электролиза.
А чем отличаются от чистых веществ их совокупности? Ответить на этот вопрос нам поможет химия. Способы разделения смесей являются физическими, поскольку они не приводят к изменению химического состава веществ. В отличие от чистых веществ, смеси имеют непостоянный состав и свойства, а разделить их можно физическими методами.
Что такое смесь
Смесью называют совокупность индивидуальных веществ. Ее примером является морская вода. В отличие от дисциллированной, она обладает горьким или соленым вкусом, кипит при более высокой, а замерзает при более низкой температуре. Способы разделения смесей веществ являются физическими. Так, из морской воды можно добыть чистую соль путем выпаривания и последующей кристаллизации.
Виды смесей
Если добавить в воду сахар, через некоторое время его частички растворятся и станут невидимыми. В результате их невозможно будет отличить невооруженным глазом. Такие смеси называют однородными, или гомогенными. Их примерами также являются воздух, бензин, бульон, духи, сладкая и соленая вода, сплав меди и алюминия. Как видите, однородные смеси могут находиться в разных агрегатных состояниях, но чаще всего встречаются жидкости. Их также называют растворами.
В результате их невозможно будет отличить невооруженным глазом. Такие смеси называют однородными, или гомогенными. Их примерами также являются воздух, бензин, бульон, духи, сладкая и соленая вода, сплав меди и алюминия. Как видите, однородные смеси могут находиться в разных агрегатных состояниях, но чаще всего встречаются жидкости. Их также называют растворами.
В неоднородных, или гетерогенных смесях можно различить частицы индивидуальных веществ. Железные и деревянные опилки, песок и поваренная соль являются их типичными примерами. Неоднородные смеси также называют взвесями. Среди них различают суспензии и эмульсии. В состав первых входит жидкость и твердое вещество. Так, эмульсией является смесь воды и песка. Эмульсией называют совокупность двух жидкостей с разной плотностью.
Существуют неоднородные смеси и со специальными названиями. Так, примером пены является пенопласт, а к аэрозолям относятся туман, дым, дезодоранты, освежители воздуха, антистатики.
Способы разделения смесей
Безусловно, многие смеси обладают более ценными свойствами, чем отдельно взятые индивидуальные вещества, входящие в их состав. Но даже в быту возникают ситуации, когда их необходимо разделить. А в промышленности на этом процессе основаны целые производства. К примеру, из нефти в результате ее переработки получают бензин, газойль, керосин, мазут, соляровое и машинное масло, ракетное топливо, ацетилен и бензол. Согласитесь, выгоднее использовать эти продукты, чем бездумн
Но даже в быту возникают ситуации, когда их необходимо разделить. А в промышленности на этом процессе основаны целые производства. К примеру, из нефти в результате ее переработки получают бензин, газойль, керосин, мазут, соляровое и машинное масло, ракетное топливо, ацетилен и бензол. Согласитесь, выгоднее использовать эти продукты, чем бездумн
Однородные смеси: определение понятия, состав, примеры
Химия изучает вещества и их свойства. При их смешивании возникают смеси, которые приобретают новые ценные качества.
Что такое смесь
Смесью называют совокупность индивидуальных веществ. Их изготовлением занимаются не только ученые в лабораториях при наличии определенных условий. Каждый день мы начинаем с ароматного чая или кофе, в который добавляем сахар. Или варим вкусный суп, который обязательно необходимо посолить. Это и есть самые настоящие смеси. Только мы об этом абсолютно не задумываемся.
Если невооруженным глазом невозможно различить частички веществ – перед вами однородные смеси (гомогенные). Их можно получить, растворяя тот самый сахар в чае или кофе.
Их можно получить, растворяя тот самый сахар в чае или кофе.
А вот если к сахару добавить песок, их частички можно различить без труда. Такую смесь считают неоднородной или гетерогенной.
Неоднородные смеси
При изготовлении смесей такого вида можно использовать вещества, находящиеся в разном агрегатном состоянии: твердом или жидком. Смесь молотого перца разного вида или другие приправы чаще всего являются именно неоднородными сухими составами.
Если в процессе приготовления гетерогенного продукта используется любая жидкость, то полученную массу называют взвесью. Причем различают их несколько видов. При смешивании жидкости с твердыми веществами образуются суспензии. Их примером является смесь воды с песком или глиной. Когда строитель изготавливает цемент, повар смешивает муку с водой, ребенок чистит зубы пастой – все они используют суспензии.
Другая разновидность гетерогенных смесей может быть получена при смешивании двух жидкостей. Естественно, если их частички различимы. Капните растительного масла в воду – и получите эмульсию.
Капните растительного масла в воду – и получите эмульсию.
Однородные смеси
Самым известным из этой группы веществ является воздух. Каждый ученик знает, что в его состав входит ряд газов: азот, кислород, двуокись углерода, водяной пар и примеси. Можно ли их рассмотреть и различить невооруженным глазом. Конечно, нет.
Таким образом, и воздух, и сладкая вода – однородные смеси. Они могут находиться в разных агрегатных состояниях. Но чаще всего используются жидкие однородные смеси. Они состоят их растворителя и растворенного вещества. Причем первым является компонент либо жидкий, либо взятый в большем объеме.
Вещества не могут растворяться в бесконечном количестве. Например, в литр воды можно добавить только два килограмма сахара. Дальше этот процесс просто не будет происходить. Такой раствор станет насыщенным.
Интересное явление представляют собой твердые гомогенные смеси. Так, водород без труда распределяется в различных металлах. Интенсивность процесса растворения зависит от многих факторов. Она увеличивается с повышением температуры жидкости и воздуха, при измельчении веществ и в результате их перемешивания.
Она увеличивается с повышением температуры жидкости и воздуха, при измельчении веществ и в результате их перемешивания.
Удивительным является тот факт, что в природе не существует абсолютно нерастворимых веществ. Даже ионы серебра распределяются между молекулами воды, образуя гомогенную смесь. Такие растворы находят широкое применение в быту и жизни человека. Например, всеми любимое и полезное молоко – однородная смесь.
Способы разделения смесей
Иногда возникает необходимость не только получить гомогенные растворы, но и разделить однородные смеси. Допустим, в доме есть только соленая вода, а нужно получить ее кристаллы отдельно. Для этого подобную массу выпаривают. Однородные смеси, примеры которых были приведены выше, чаще всего разделяют именно таким способом.
На основе различий в температуре кипения основана дистилляция. Всем известно, что вода начинает испаряться при 100 градусах по Цельсию, а этиловый спирт – при 78. Смесь данных жидкостей нагревают. Сначала испаряются пары спирта. Их конденсируют, то есть переводят в жидкое состояние, соприкасая с любой охлажденной поверхностью.
Их конденсируют, то есть переводят в жидкое состояние, соприкасая с любой охлажденной поверхностью.
При помощи магнита разделяют смеси, в состав которых входят металлы. Например, железные и деревянные опилки. Растительное масло и воду отдельно можно получить при помощи отстаивания.
Гетерогенные и однородные смеси, примеры которых проиллюстрированы в статье, имеют важное хозяйственное значение. Полезные ископаемые, воздух, подземные воды, моря, пищевые продукты, строительные материалы, напитки, пасты – все это совокупность индивидуальных веществ, без которых жизнь была бы просто невозможна.
Соединения и смеси
Большинство веществ состоит из нескольких элементов, т.е. многие вещества представляют собой соединения или смеси. Соединение — это вещество, содержащее атомы двух или более элементов, соединенные между собой химической связью. В смеси, например в морской воде или воздухе, различные вещества перемешаны, но не связаны химически. Морской песок — смесь частиц кварки, раковин и органических веществ (см. рис.). Кварц – соединение кремния и кислорода. Почти бесцветные песчинки – это частицы кварца.
рис.). Кварц – соединение кремния и кислорода. Почти бесцветные песчинки – это частицы кварца.
Соединения
В соединении атомы двух или более элементов связаны вместе химической связью, так что образуется совершенно новое вещество. Углекислый газ — это соединение, состоящее из связанных атомов углерода и кислорода.
Соединение нельзя разделить на элементы физическими методами, например путем фильтрации или выпаривания. Свойства соединения отличаются от свойств элементов. Если нагреть смесь железа с серой (слева), то произойдет реакция и образуется новое вещество – сульфид железа. После реакции железо уже нельзя отделить от серы. В отличие от железа сульфид железа не намагничивается, а в отличие от измельченной серы, тонет в воде. В каждом образце соединения элементы содержатся в одинаковой пропорции. Химическая формула отражает соотношение элементов. Формула сульфида железа FeS говорит о том, что каждый атом железа связан с одним атомом серы. Вода — это соединение водорода с кислородом. Стекло — соединение кальция, кремния, кислорода и натрии. Соединения делятся на группы в соответствии с их химическими свойствами. Так, кислоты и основания составляют особые группы. Соединения можно также разделить по признаку наличия тех или иных атомов. Например, гидриды — это вещества, содержащие водород. Хлориды содержат хлор, оксиды содержат кислород. При реакция натрия с хлором, образуется хлорид натрия — поваренная соль. Хлор — ядовитый газ, а натрий — очень активный металл. Хлорид натрия не обладает этими опасными свойствами.
Вода — это соединение водорода с кислородом. Стекло — соединение кальция, кремния, кислорода и натрии. Соединения делятся на группы в соответствии с их химическими свойствами. Так, кислоты и основания составляют особые группы. Соединения можно также разделить по признаку наличия тех или иных атомов. Например, гидриды — это вещества, содержащие водород. Хлориды содержат хлор, оксиды содержат кислород. При реакция натрия с хлором, образуется хлорид натрия — поваренная соль. Хлор — ядовитый газ, а натрий — очень активный металл. Хлорид натрия не обладает этими опасными свойствами. Все органические соединения содержат углерод. Все живые организмы, как и ископаемое топливо, например нефть, состоят из органических соединений. Люди также производят органические соединения — пластмассы, красители, моющие средства, лекарства.
Смеси
Большинство окружающих нас веществ — смеси.
Они содержат различные вещества (элементы или соединения), не вступившие в химические реакции. Смесь может содержать два или более элементов — веществ, состоящих из атомов одного типа. Смесь может содержать соединения, т.е. вещества, состоящие из атомов разных типов. Смесь может состоять из элементов и соединений. Воздух — смесь элементов (кислород) и соединений (пыль, копоть). Компоненты смеси химически не связаны, и их можно легко разделить. Например, из смеси железа с серой частицы железа можно извлечь магнитом. Частицы железа притягиваются к магниту (см. рис.), а частицы серы на магнит не реагируют. В смеси компоненты могут содержаться в любых пропорциях. Все компоненты сохраняют свои индивидуальные свойства. Тесто — это смесь различных соединений: яиц, муки, жира. Испеченный пирог представляет собой новое соединение. Соль — это соединение натрия с хлором. Масло — органическое соединение, в нем есть углерод, водород и кислород
Смесь может содержать два или более элементов — веществ, состоящих из атомов одного типа. Смесь может содержать соединения, т.е. вещества, состоящие из атомов разных типов. Смесь может состоять из элементов и соединений. Воздух — смесь элементов (кислород) и соединений (пыль, копоть). Компоненты смеси химически не связаны, и их можно легко разделить. Например, из смеси железа с серой частицы железа можно извлечь магнитом. Частицы железа притягиваются к магниту (см. рис.), а частицы серы на магнит не реагируют. В смеси компоненты могут содержаться в любых пропорциях. Все компоненты сохраняют свои индивидуальные свойства. Тесто — это смесь различных соединений: яиц, муки, жира. Испеченный пирог представляет собой новое соединение. Соль — это соединение натрия с хлором. Масло — органическое соединение, в нем есть углерод, водород и кислородВиды смесей
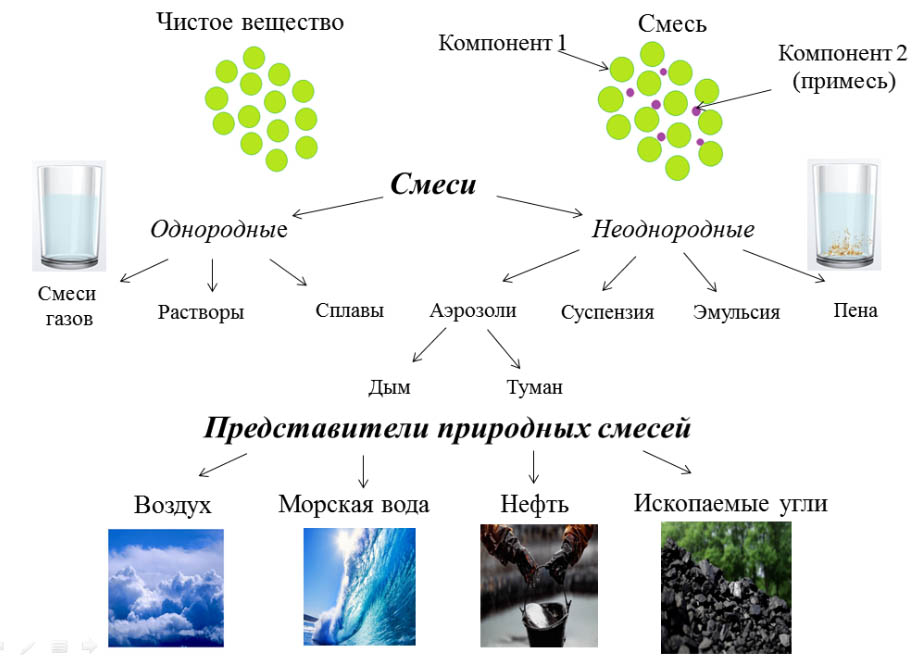 Латунь — смесь двух твердых веществ, меди и цинка. Смеси металлов называются сплавами. Когда твердое вещество (например, соль) растворяется в жидкости (например, в воде), образуется раствор. Легко растворяющееся твердое вещество называют растворимым, а то, которое не растворяется, — нерастворимым. Смесь, состоящую из частиц твердого вещества, взвешенных в жидкости или газе, называют взвесью. Кровь, молоко, дым — все это взвеси. Молоко — взвесь частиц жира в воде. Шипучие напитки — смеси двух жидкостей (воды и красителя) и углекислого газа. Газ выделяется в виде пузырьков. Жидкости, которые легко образуют смеси, например вода и чернила, называются смешиваемыми. Если жидкости не образуют раствора — вода и нефть, — говорят, что они несмешиваемые. Чтобы их перемешать, нужно добавить третье вещество – эмульгатор. Эмульгатор разбивает нефть на небольшие капли, зависающие в воде. Полученная смесь называется эмульсией.
Латунь — смесь двух твердых веществ, меди и цинка. Смеси металлов называются сплавами. Когда твердое вещество (например, соль) растворяется в жидкости (например, в воде), образуется раствор. Легко растворяющееся твердое вещество называют растворимым, а то, которое не растворяется, — нерастворимым. Смесь, состоящую из частиц твердого вещества, взвешенных в жидкости или газе, называют взвесью. Кровь, молоко, дым — все это взвеси. Молоко — взвесь частиц жира в воде. Шипучие напитки — смеси двух жидкостей (воды и красителя) и углекислого газа. Газ выделяется в виде пузырьков. Жидкости, которые легко образуют смеси, например вода и чернила, называются смешиваемыми. Если жидкости не образуют раствора — вода и нефть, — говорят, что они несмешиваемые. Чтобы их перемешать, нужно добавить третье вещество – эмульгатор. Эмульгатор разбивает нефть на небольшие капли, зависающие в воде. Полученная смесь называется эмульсией.
Разделение смесей
Химики знают много способов разделение смесей на составные части. Выбор способа зависит от вида смеси. Простейший способ отделения твердых частиц, взвешенных в жидкости, — оставить взвесь в покое, чтобы частицы осели на дно. В мутной воде есть частицы песка, почвы, органических веществ, но они постепенно оседают на дно. Другой способ отделения твердых частиц от жидкости — фильтрация. Фильтр задерживает твердые частицы и пропускает молекулы жидкости. Этот метод используется на водонапорных станциях для получения чистой питьевой воды. Жидкость, прошедшая через фильтр, — фильтрат; твердые частицы, задержанные фильтром, — осадок.
Для определения состава смеси используется хроматография. Смесь растворяется в растворителе, и часть ее помещается на бумажный фильтр, который задерживает разные вещества в разной степени. На фильтре образуются цветные полосы — хроматограмма. Исследователь определяет состав смеси, сравнивая ее хроматограмму с хроматограммами известных веществ. Хроматография помогает установить, какие красители добавлены в продукт.
Выпаривание — это способ выделения твердого вещества из жидкого раствора. Раствор разогревают, он закипает, жидкость испаряется и на дне остается твёрдое вещество. Лимонный сок — водный раствор лимонной кислоты. Если сок кипятить, вода испарится и на дне кастрюли останутся кристаллы лимонной кислоты. Дистилляция
 В специальной машине — центрифуге — сосуд с жидкостью очень быстро вращается. Центробежная сила отбрасывает твердые частицы к стенкам сосуда, после чего жидкость сливают или фильтруют. Пример центрифуги — сушильный барабан. В медицине центрифугу используют для отделения красных кровяных телец от крови, которая представляет собой взвесь кровяных пластинок и красных и белых телец в особой жидкости — плазме.
В специальной машине — центрифуге — сосуд с жидкостью очень быстро вращается. Центробежная сила отбрасывает твердые частицы к стенкам сосуда, после чего жидкость сливают или фильтруют. Пример центрифуги — сушильный барабан. В медицине центрифугу используют для отделения красных кровяных телец от крови, которая представляет собой взвесь кровяных пластинок и красных и белых телец в особой жидкости — плазме.|
Агрегатное состояние составных частей
(до образования смеси) |
Гомогенная смесь
(гомогенная система) |
Гетерогенная смесь
(гетерогенная система) |
|---|---|---|
| Твёрдое — твёрдое | Твёрдые растворы, сплавы (например латунь, бронза) |
Горные породы (например гранит, минералосодержащие руды и др. ) ) |
| Твёрдое — жидкое | Жидкие растворы (например, водные растворы солей) | Твёрдое в жидком — суспензии или взвеси (например, частицы глины в воде, коллоидные растворы ) |
| Жидкое в твёрдом — жидкость в пористых телах (например, почвы, грунты) | ||
| Твёрдое — газообразное | Хемосорбированный водород в платине, палладии, сталях | Твёрдое в газообразном — порошки, аэрозоли, в том числе дым, пыль, смог |
| Газообразное в твёрдом — пористые материалы (например, кирпич, пемза) | ||
| Жидкое — твёрдое | Твёрдые жидкости (например, стекло — твёрдое, но всё же жидкость) | Может принимать разную форму и фиксировать её (например, посуда — разной формы и цвета) |
| Жидкое — жидкое | Жидкие растворы (например, уксус — раствор уксусной кислоты в воде) | Двух- и многослойные жидкие системы, эмульсии (например, молоко — капли жидкого жира в воде) |
| Жидкое — газообразное | Жидкие растворы (например, раствор диоксида углерода в воде) | Жидкое в газообразном — аэрозоли жидкости в газе, в том числе туманы |
| Газообразное в жидком — пены (например, мыльная пена) | ||
| Газообразное — газообразное |
Газовые растворы (смеси любых количеств и любого числа газов), напр. воздух . воздух . |
Гетерогенная система невозможна |
Смесь, в которой даже с помощью увеличительных приборов нельзя увидеть частицы составляющих ее веществ, называется однородной или гомогенной.
⇐ ПредыдущаяСтр 10 из 11Следующая ⇒Однородные смеси по агрегатному состоянию делятся на газообразные, жидкие и твердые.
Смесь любых газов всегда гомогенна. Например, чистый воздух – это гомогенная смесь азота, кислорода, углекислого и благородных газов, водяных паров. А вот пыльный воздух – это уже гетерогенная смесь тех же газов, только содержащая еще и частицы пыли. Вам наверняка доводилось не раз видеть, как ранним утром через неплотно задернутые шторы в комнату пробиваются солнечные лучи. Пути их нередко бывают отмечены светящимися дорожками: это взвешенные в воздухе частички пыли рассеивают солнечный свет. Смог над городом или над промышленным предприятием – это тоже гетерогенная смесь: воздух, в котором содержатся не только частицы пыли, но также сажа из дыма, капельки различных жидкостей и др.
| Рис. 61. Смог над промышленным предприятием |
Природный газ, попутный нефтяной газ также представляют собой природные смеси газообразных веществ, основным компонентом которых является метан СН4. Тот же метан поступает в наши квартиры по трубопроводам и горит на кухне веселым голубым пламенем. Но бытовойгаз – это тоже смесь. В ее состав специально вводят резко пахнущие вещества, чтобы можно было по запаху почувствовать малейшую утечку газа. Для чего это необходимо? Дело в том, что и воздух (необходимый для дыхания всего живого), и природный газ (незаменимое топливо и сырье для химической отрасли промышленности) – это великое благо человечества, но их смесь превращается в грозную разрушительную силу из-за чрезвычайной взрывоопасности. Из сообщений средств массовой информации вы, безусловно, знаете о трагедиях, связанных со взрывами метана в угольных шахтах, взрывами бытового газа в результате преступной халатности или несоблюдения элементарных норм безопасности. Почувствовав запах газа в квартире или в подъезде своего дома, вы должны немедленно перекрыть краны и вентили, проветрить помещение, по телефону 04 вызвать специализированную аварийную службу.При этом категорически запрещается пользоваться открытым огнем, включать или выключать электроприборы.
Почувствовав запах газа в квартире или в подъезде своего дома, вы должны немедленно перекрыть краны и вентили, проветрить помещение, по телефону 04 вызвать специализированную аварийную службу.При этом категорически запрещается пользоваться открытым огнем, включать или выключать электроприборы.
К жидким природным смесям относится нефть. В ее состав входят сотни различных компонентов, главным образом соединения углерода. Нефть называют «кровью Земли», «черным золотом», и вам хорошо известно, насколько значительную роль в экономике нашего государства и многих других стран играют добыча, переработка и экспорт нефти и нефтепродуктов.
Безусловно, самой распространенной жидкой смесью, а точнее раствором, является вода морей и океанов. Вы уже знаете, что в одном литре морской воды в среднем содержится 35 г солей, основная часть из которых приходится на хлорид натрия. В отличие от чистой воды морская имеет горько-соленый вкус, замерзает не при 0 °С, а при –1,9 °С.
С жидкими смесями в повседневной жизни вы сталкиваетесь постоянно. Шампуни и напитки, микстуры и препараты бытовой химии – все это смеси веществ. Даже воду из-под крана нельзя считать чистым веществом: в ней содержатся растворенные соли, мельчайшие нерастворимые примеси, ее обеззараживают хлорированием. Такую воду нельзя пить некипяченой, ее не рекомендуют использовать для приготовления пищи. Специальные бытовые фильтры помогут очистить водопроводную воду не только от твердых частиц, но и от некоторых растворенных примесей. Даже растворы реактивов на водопроводной воде готовить нельзя. Воду для этого очищают методом дистилляции, о чем вы узнаете немного позже.
Широко распространены и твердые смеси. Как мы уже говорили, горные породы представляют собой смеси нескольких веществ. Почва, глина, песок – это тоже смеси. К твердым смесям можно отнести стекло, керамику, сплавы. Каждому знакомы кулинарные смеси или смеси, образующие стиральные порошки.
Скажите, одинаков ли состав воздуха, который мы вдыхаем и выдыхаем? Конечно, нет. В последнем становится меньше кислорода, зато больше углекислого газа. Но «больше-меньше» – понятия относительные. Состав смесей можно выразить количественно, т.е. в цифрах. Как? Об этом речь пойдет в следующем параграфе.
1. В чем отличие материала от химического вещества?
2. Может ли вода в различных агрегатных состояниях быть материалом? Приведите примеры.
3. Что такое смесь? Приведите примеры природных смесей различного агрегатного состояния. Назовите компоненты этих смесей.
4. Приведите примеры бытовых смесей различного агрегатного состояния. Назовите компоненты этих смесей.
5. Какие смеси называют гетерогенными? Приведите примеры таких природных и бытовых смесей и назовите их компоненты.
6. Какие смеси называют гомогенными? Приведите примеры таких природных и бытовых смесей и назовите их компоненты.
7. Какой воздух можно рассматривать как гомогенную смесь, а какой – как гетерогенную?
Глава 2. Математика в химии
(окончание)
Объемная доля газов в смеси
В состав воздуха входит несколько различных газов: кислород, азот, углекислый газ, благородные газы, водяные пары и некоторые другие вещества. Содержание каждого из этих газов в чистом воздухе строго определенно.
Для того чтобы выразить состав смеси газов в цифрах, т.е. количественно, используют особую величину, которую называют объемной долей газов в смеси.
Объемную долю газа в смеси обозначают греческой буквой – «фи».
Объемной долей газа в смеси называют отношение объема данного газа к общему объему смеси:
Что же показывает объемная доля газа в смеси или, как говорят, какой физический смысл этой величины? Объемная доля газа показывает, какую часть общего объема смеси занимает данный газ.
Если бы нам удалось разделить 100 л воздуха на отдельные газообразные компоненты, мы получили бы около 78 л азота, 21 л кислорода, 30 мл углекислого газа, в оставшемся объеме содержались бы так называемые благородные газы (главным образом аргон) и некоторые другие (рис. 62).
| Рис. 62. Состав атмосферного воздуха |
Рассчитаем объемные доли этих газов в воздухе:
Нетрудно заметить, что сумма объемных долей всех газов в смеси всегда равна 1, или 100%:
(азота) + (кисл.) + (угл. газа) + (др. газов) = 78% + 21% + 0,03% + 0,97% = 100%.
Тот воздух, который мы выдыхаем, гораздо беднее кислородом (его объемная доля снижается до 16%), зато содержание углекислого газа возрастает до 4%. Такой воздух для дыхания уже непригоден. Вот почему помещение, в котором находится много людей, надо регулярно проветривать.
В химии на производстве чаще приходится сталкиваться с обратной задачей: определять объем газа в смеси по известной объемной доле.
Пример. Вычислите объем кислорода, содержащегося в 500 л воздуха.
Из определения объемной доли газа в смеси выразим объем кислорода:
V(кисл.) = V(возд.)• (кисл.).
Подставим в уравнение числа и рассчитаем объем кислорода:
V(кисл.) = 500 (л)•0,21 = 105 л.
Кстати, для приближенных расчетов объемную долю кислорода в воздухе можно принять равной 0,2, или 20%.
При расчете объемных долей газов в смеси можно воспользоваться маленькой хитростью. Зная, что сумма объемных долей равна 100%, для «последнего» газа в смеси эту величину можно рассчитать по-другому.
Задача.Анализ атмосферы Венеры показал, что в 50 мл венерианского «воздуха» содержится 48,5 мл углекислого газа и 1,5 мл азота. Рассчитайте объемные доли газов в атмосфере планеты.
Дано:
V(смеси) = 50 мл,
V(угл. газа) = 48,5 мл,
V(азота) = 1,5 мл.
Найти:
(угл. газа),
(азота).
Решение
Рассчитаем объемную долю углекислого газа в смеси. По определению:
Вычислим объемную долю азота в смеси, зная, что сумма объемных долей газов в смеси равна 100%:
(угл. газа) + (азота) = 100%,
(азота) = 100% – (угл. газа) = 100% – 97% = 3%.
Ответ. (угл. газа) = 97%, (азота) = 3%.
С помощью какой величины измеряют содержание компонентов в смесях другого типа, например в растворах? Понятно, что в этом случае пользоваться объемной долей неудобно. На помощь приходит новая величина, о которой вы узнаете на следующем уроке.
1. Что такое объемная доля компонента в газовой смеси?
2. Объемная доля аргона в воздухе 0,9%. Какой объем воздуха необходим для получения 5 л аргона?
3. При разделении воздуха было получено 224 л азота. Какие объемы кислорода и углекислого газа были получены при этом?
Какие объемы кислорода и углекислого газа были получены при этом?
4. Объемная доля метана в природном газе составляет 92%. Какой объем этой газовой смеси будет содержать 4,6 мл метана?
5. Смешали 6 л кислорода и 2 л углекислого газа. Найдите объемную долю каждого газа в полученной смеси.
Читайте также:
Разделение смесей. Очистка веществ. Фильтрование.
Чистые вещества и смеси
Мы живем среди химических веществ. Мы вдыхаем воздух, а это смесь газов (азота, кислорода и других), выдыхаем углекислый газ. Умываемся водой — это еще одно вещество, самое распространенное на Земле. Пьём молоко — смесь воды с мельчайшими капельками молочного жира, и не только: здесь еще есть молочный белок казеин, минеральные соли, витамины и даже сахар, но не тот, с которым пьют чай, а особый, молочный — лактоза. Едим яблоки, которые состоят из целого набора химических веществ — здесь и сахар, и яблочная кислота, и витамины. .. Когда прожеванные кусочки яблока попадают в желудок, на них начинают действовать пищеварительные соки человека, которые помогают усваивать все вкусные и полезные вещества не только яблока, но и любой другой пищи. Мы не только живем среди химических веществ, но и сами из них состоим. Каждый человек — его кожа, мышцы, кровь, зубы, кости, волосы построены из химических веществ, как дом из кирпичей. Азот, кислород, сахар, витамины — вещества природного, естественного происхождения. Стекло, резина, сталь – это тоже вещества, точнее, материалы (смеси веществ). И стекло, и резина — искусственного происхождения, в природе их не было. Совершенно чистые вещества в природе не встречаются или встречаются очень редко.
.. Когда прожеванные кусочки яблока попадают в желудок, на них начинают действовать пищеварительные соки человека, которые помогают усваивать все вкусные и полезные вещества не только яблока, но и любой другой пищи. Мы не только живем среди химических веществ, но и сами из них состоим. Каждый человек — его кожа, мышцы, кровь, зубы, кости, волосы построены из химических веществ, как дом из кирпичей. Азот, кислород, сахар, витамины — вещества природного, естественного происхождения. Стекло, резина, сталь – это тоже вещества, точнее, материалы (смеси веществ). И стекло, и резина — искусственного происхождения, в природе их не было. Совершенно чистые вещества в природе не встречаются или встречаются очень редко.
Каждое вещество всегда содержит определенное количество примесей. Вещество, в котором почти нет примесей, называют чистым. С такими веществами работают в научной лаборатории, школьном химическом кабинете. Заметим, что абсолютно чистых веществ не существует.
Индивидуальное чистое вещество обладает определённым набором характеристических свойств (постоянными физическими свойствами). Только чистая дистиллированная вода имеет tпл = 0 °С, tкип= 100 °С, не имеет вкуса. Морская вода замерзает при более низкой, а закипает при более высокой температуре, вкус у нее горько-соленый. Вода Черного моря замерзает при более низкой, а закипает при более высокой температуре, чем вода Балтийского моря. Почему? Дело в том, что в морской воде содержатся другие вещества, например растворенные соли, т.е. она представляет собой смесь различных веществ, состав которой меняется в широких пределах, свойства же смеси не являются постоянными. Определение понятия «смесь» было дано в XVII в. английским ученым Робертом Бойлем: «Смесь — целостная система, состоящая из разнородных компонентов».
Только чистая дистиллированная вода имеет tпл = 0 °С, tкип= 100 °С, не имеет вкуса. Морская вода замерзает при более низкой, а закипает при более высокой температуре, вкус у нее горько-соленый. Вода Черного моря замерзает при более низкой, а закипает при более высокой температуре, чем вода Балтийского моря. Почему? Дело в том, что в морской воде содержатся другие вещества, например растворенные соли, т.е. она представляет собой смесь различных веществ, состав которой меняется в широких пределах, свойства же смеси не являются постоянными. Определение понятия «смесь» было дано в XVII в. английским ученым Робертом Бойлем: «Смесь — целостная система, состоящая из разнородных компонентов».
Смесями являются почти все природные вещества, продукты питания (кроме соли, сахара, некоторых других), многие лекарственные и косметические средства, товары бытовой химии, строительные материалы.
Признаки сравнения | Чистое вещество | Смесь |
Состав | Постоянный | Непостоянный |
Вещества | Одно и то же | Различные |
Физические свойства | Постоянные | Непостоянные |
Изменение энергии при образовании | Происходит | Не происходит |
Разделение | С помощью химических реакций | Физическими методами |
Каждое вещество, содержащееся в смеси, называют компонентом.
Существуют однородные и неоднородные смеси.
Добавим небольшую порцию сахара в стакан с водой и будем перемешивать, пока весь сахар не растворится. Жидкость будет иметь сладкий вкус. Таким образом, сахар не исчез, а остался в смеси. Ho его кристалликов мы не увидим, даже рассматривая каплю жидкости в мощный микроскоп. Приготовленная смесь сахара и воды является однородной в ней равномерно перемешаны мельчайшие частицы этих веществ.
Большинство металлических сплавов — также однородные смеси. Например, в сплаве золота с медью (его используют для изготовления ювелирных украшений) отсутствуют красные частицы меди и желтые частицы золота.
Из материалов, которые являются однородными смесями веществ, изготовляют много предметов разнообразного назначения.
К однородным смесям принадлежат все смеси газов, в том числе и воздух. Существует немало однородных смесей жидкостей.
Однородные смеси еще называют растворами, даже если они твердые или газообразные.
Приведём примеры растворов (воздух в колбе, поваренная соль + вода, разменная монета: алюминий + медь или никель + медь).
Вам известно, что мел не растворяется в воде. Если его порошок всыпать в стакан с водой, то в образовавшейся смеси всегда можно обнаружить частицы мела, которые видны невооруженным глазом или в микроскоп.
К неоднородным смесям относятся большинство минералов, почва, строительные материалы, живые ткани, мутная вода, молоко и другие продукты питания, некоторые лекарственные и косметические средства.
В неоднородной смеси физические свойства компонентов сохраняются. Так, железные опилки, смешанные с медными или алюминиевыми, не теряют способности притягиваться к магниту.
Некоторые виды неоднородных смесей имеют специальные названия: пена (например, пенопласт, мыльная пена), суспензия (смесь воды с небольшим количеством муки), эмульсия (молоко, хорошо взболтанные растительное масло с водой), аэрозоль (дым, туман).
Способы разделения смесей
В природе вещества существуют в виде смесей. Для лабораторных исследований, промышленных производств, для нужд фармакологии и медицины нужны чистые вещества.
Существует много методов разделения смесей. Их выбирают, учитывая тип смеси, агрегатное состояние и различия в физических свойствах компонентов.
Эти способы основаны на различиях в физических свойствах компонентов смеси.
Рассмотрим способы разделения гетерогенных и гомогенных смесей.
Пример смеси | Способ разделения |
Суспензия — смесь речного песка с водой | Отстаивание Разделение отстаиванием основано на различных плотностях веществ. Более тяжелый песок оседает на дно. Так же можно разделить и эмульсию: отделить нефть или растительное масло от воды. В лаборатории это можно сделать с помощью делительной воронки. Нефть или растительное масло образует верхний, более легкий слой. В результате отстаивания выпадает роса из тумана, осаждается сажа из дыма, отстаиваются сливки в молоке. |
Смесь песка и поваренной соли в воде | Фильтрование Разделение гетерогенных смесей с помощью фильтрования основано на различной растворимости веществ в воде и на различных размерах частиц. Через поры фильтра проходят лишь соизмеримые с ними частицы веществ, в то время как более крупные частицы задерживаются на фильтре. Так можно разделить гетерогенную смесь поваренной соли и речного песка. В качестве фильтров можно использовать различные пористые вещества: вату, уголь, обожженную глину, прессованное стекло и другие. Способ фильтрования — это основа работы бытовой техники, например пылесосов. Его используют хирурги – марлевые повязки; буровики и рабочие элеваторов — респираторные маски. С помощью чайного ситечка для фильтрования чаинок Остапу Бендеру — герою произведения Ильфа и Петрова — удалось забрать один из стульев у Эллочки Людоедки («Двенадцать стульев»). |
Смесь порошка железа и серы | Действие магнитом или водой Порошок железа притягивался магнитом, а порошок серы — нет. Несмачивающийся порошок серы всплывал на поверхность воды, а тяжелый смачивающийся порошок железа оседал на дно. |
Раствор соли в воде — гомогенная смесь | Выпаривание или кристаллизация Вода испаряется, а в фарфоровой чашке остаются кристаллы соли. При выпаривании воды из озер Эльтон и Баскунчак получают поваренную соль. Этот способ разделения основан на различии в температурах кипения растворителя и растворенного вещества. Если вещество, например сахар, разлагается при нагревании, то воду испаряют неполностью — упаривают раствор, а затем из насыщенного раствора осаждают кристаллы сахара. Иногда требуется очистить от примесей растворители с меньшей температурой кипения, например воду от соли. В этом случае пары вещества необходимо собрать и затем сконденсировать при охлаждении. Такой способ разделения гомогенной смеси называется дистилляцией, или перегонкой. В специальных приборах — дистилляторах получают дистиллированную воду, которую используют для нужд фармакологии, лабораторий, систем охлаждения автомобилей. В домашних условиях можно сконструировать такой дистиллятор. Если же разделять смесь спирта и воды, то первым будет отгоняться (собираться в пробирке-приемнике) спирт с tкип = 78 °С, а в пробирке останется вода. Перегонка используется для получения бензина, керосина, газойля из нефти. |
Особым методом разделения компонентов, основанным на различной поглощаемости их определенным веществом, является хроматография.
Если подвесить полоску из фильтровальной бумаги над сосудом с красными чернилами, погружая в них лишь конец полоски. Раствор впитывается бумагой и поднимается по ней. Но граница подъема краски отстает от границы подъема воды. Так происходит разделение двух веществ: воды и красящего вещества в чернилах.
С помощью хроматографии русский ботаник М. С. Цвет впервые выделил хлорофилл из зеленых частей растений. В промышленности и лабораториях вместо фильтровальной бумаги для хроматографии используют крахмал, уголь, известняк, оксид алюминия. А всегда ли требуются вещества с одинаковой степенью очистки?
Для различных целей необходимы вещества с различной степенью очистки. Воду для приготовления пищи достаточно отстоять для удаления примесей и хлора, используемого для ее обеззараживания. Воду для питья нужно предварительно прокипятить. А в химических лабораториях для приготовления растворов и проведения опытов, в медицине необходима дистиллированная вода, максимально очищенная от растворенных в ней веществ. Особо чистые вещества, содержание примесей в которых не превышает одной миллионной процента, применяются в электронике, в полупроводниковой, ядерной технике и других точных отраслях промышленности.
5 готовых смесей | Стандартное руководство пользователя
- Стандартное руководство пользователя
- Обзор
- Об этом руководстве пользователя
- Интернет-ресурсы
- Благодарности
- Авторское право, товарный знак и лицензирование
- Часть 1. Примеры моделей
- 1 Регрессионные модели
- 1,1 Линейная регрессия
- Матричная запись и векторизация
- 1.2 Репараметризация QR
- 1,3 Приоры для коэффициентов и масштабов
- 1,4 Устойчивые шумовые модели
- 1,5 Логистическая и пробит-регрессия
- 1,6 Мультилогитовая регрессия
- Ограничения на объявления данных
- Идентифицируемость
- 1,7 Параметрирование центрированных векторов
- \ (K-1 \) Степени свободы
- QR-разложение
- Симплекс с преобразованием и масштабированием
- Мягкое центрирование
- 1.8 Упорядоченная логистика и пробит-регрессия
- Упорядоченная логистическая регрессия
- 1,1 Линейная регрессия
Добавьте сюда свой ответ.Проверьте некоторые подобные вопросы!Классифицируйте каждую из смесей. [2 ответа]Классифицируйте каждую из следующих смесей как настоящий раствор, коллоид или суспензию. 1) песок / водная взвесь 2) сахар / вода-раствор 3) дым-коллоид 4) яичный белок коллоидный сырой, суспензия 5) сливки взбитые-коллоидные Мне это понравилось .. Помогите пожалуйста! Спасибо 2-х тактные топливные смеси [1 ответ]У меня есть старый газовый триммер Craftsman.Это требует топливной смеси 16: 1. Можно ли использовать сегодняшнее масло для двухтактных двигателей в соотношении 50: 1? Тот же вопрос относится к старой бензопиле Homelite Super2. Спасибо, Фил. 3 примера [2 ответа]Какие 3 примера, как Кейси Энтони продолжает говорить в прошедшем времени о своей дочери Кейли Посмотреть еще вопросы Поиск |
Смеси | Классификация вещества
2.2 смеси (ESAW)
В повседневной жизни мы постоянно видим смеси. Тушеное мясо, например, представляет собой смесь различных продуктов, таких как мясо и овощи; морская вода представляет собой смесь воды, соли и других веществ, а воздух — смесь газов, таких как углекислый газ, кислород и азот.
- Смесь
Смесь — это комбинация двух или более веществ, в которой эти вещества не связаны (или не соединены) друг с другом, и между ними не происходит химической реакции.
В смеси, вещества, входящие в состав смеси:
не в фиксированном соотношении
Представьте, например, что у вас есть \ (\ text {250} \) \ (\ text {mL} \) воды и вы добавляете в воду песок. Неважно, добавляете ли вы \ (\ text {20} \) \ (\ text {g} \), \ (\ text {40} \) \ (\ text {g} \), \ (\ text {100} \) \ (\ text {g} \) или любую другую массу песка в воду; его по-прежнему будут называть смесью песка и воды.
сохраняют свои физические свойства
В примере, который мы использовали для песка и воды, ни одно из этих веществ не изменилось никаким образом при их смешивании. Песок — это еще песок, а вода — еще вода.
можно разделить механическими средствами
Разделение чего-либо «механическими средствами» означает отсутствие химического процесса.В нашем примере с песком и водой можно разделить смесь, просто пропустив воду через фильтр. Что-то физическое сделано со смесью, а не что-то химическое .
Мы можем дополнительно сгруппировать смеси, разделив их на неоднородные и однородные.
Гетерогенные смеси (ESAX)
Гетерогенная смесь не имеет определенного состава.Крупа в молоке — пример неоднородной смеси. Другой пример — почва. В почве есть галька, растительное вещество и песок. Хотя вы можете добавлять одно вещество к другому, они останутся в смеси отдельными. Мы говорим, что эти гетерогенные смеси неоднородны , другими словами, они не совсем одинаковы во всем.
Злаки
Рис. 2.2: Субмикроскопическое изображение гетерогенной смеси. Серые круги — это одно вещество (например,грамм. один злак), а белые кружки — другое вещество (например, другой злак). Фон — молоко.
- Гетерогенная смесь
Гетерогенная смесь — это смесь, состоящая из двух или более веществ. Он неоднороден, и на нем видны разные компоненты смеси.
Гетерогенные смеси могут быть дополнительно подразделены в зависимости от того, являются ли они смешанными двумя жидкостями: твердым и жидким, или жидким и газовым, или даже газом и твердым телом.Этим смесям даны специальные названия, которые вы можете увидеть в таблице ниже.
Фазы вещества | Название смеси | Пример | |||
жидкость-жидкость | жидкость-жидкость | 11 9011 9011 9011 9013 | твердое вещество-жидкость | суспензия | мутная вода |
газ-жидкость | аэрозоль | газированные напитки 3 | смог |
Таблица 2.1: Примеры различных гетерогенных смесей
Гомогенные смеси (ESAY)
Гомогенная смесь имеет определенный состав и определенные свойства. В однородной смеси не видны разные части. Раствор соли в воде является примером гомогенной смеси. Когда соль растворяется, она равномерно распространяется по воде, так что все части раствора одинаковы, и вы больше не можете видеть соль отдельно от воды.Подумайте также о кофе без молока. Воздух, которым мы дышим, является еще одним примером гомогенной смеси, поскольку он состоит из разных газов, которые находятся в постоянном соотношении и которые нельзя визуально отличить друг от друга (то есть вы не можете видеть разные компоненты).
Кофе
Соль, растворяющаяся в воде
Сплав представляет собой гомогенную смесь двух или более элементов, по крайней мере, один из которых является металлом, причем полученный материал имеет металлические свойства.Например, сталь — это сплав, состоящий из
Слово «смесь» можно определить как гетерогенная ассоциация веществ, которые не могут быть представлены одной химической формулой. Это определение не ограничивает смеси твердыми веществами. смешанные с жидкостями, и не каждая смесь считается быть решением. Два или более газов, твердых частиц или жидкости могут быть смешаны, а две и более разных фазы вещества могут быть объединены в смесь.Биолог должен уметь работать с разнообразными смесей, многие, но не все, из которых сделаны путем смешивания твердого вещества с водой. Не все такие смеси также являются истинными растворами. Вот вот несколько примеров смесей, которые биолог может встретиться в лаборатории.
Вильгельм Оствальд, лауреат Нобелевской премии по химии в 1909 г. был одним из основоположников современной физической химия.Сообщается, что он сказал: «Там нет резких отличий между механическими подвесками, коллоидные растворы и молекулярные [истинные] растворы. Происходит постепенный и непрерывный переход от от первого до второго до третьего ». А смесь, независимо от типа, описывается как «равномерно рассредоточены ». Это означает, что один или несколько второстепенных компоненты равномерно распределены по основной компонент.Главный компонент — это вещество это присутствует в наибольшей пропорции. В Биологическая лаборатория часто является основным компонентом жидкость, второстепенные компоненты могут быть твердыми, другие жидкости или даже газы. «Механическая подвеска», к которой Упомянутый Оствальд описать проще всего. В второстепенный компонент в суспензии обычно виден в оптический микроскоп и часто виден невооруженным глазом.Коллоидная смесь иногда называется коллоидной системой, коллоидной суспензией, или просто «коллоид». Наименьшее измерение второстепенного компонента коллоидной смеси может диапазон примерно от одного нанометра (1 миллиардная метра) до одного микрометра (1 миллионная часть метр). Примеры жидких коллоидных смесей: молоко, краски и мутная вода. Среда может быть газ, в случае смога, дыма или аэрозоля спреи.Некоторые твердые вещества считаются коллоидными. смеси, как из стали, так и из поролона. В истинном растворе один или второстепенные компоненты взаимодействуют на молекулярном или ионном уровне с основной компонент. Минорные компоненты — атомы или молекулы, и не различимы ни в одном оптический микроскоп. Научитесь применять правильный термин при описании смеси. Например, смешивание клетки в буфере обычно не дают решения.Растворы представляют собой полностью однородные смеси, свойство, которое часто приписывают приостановкам а также коллоиды. Незначительные компоненты истинное решение, однако, остается рассредоточенным из-за взаимодействия на молекулярном уровне. Вещество считается растворимым в определенном растворителе если он способен взаимодействовать с растворителем так, чтобы сформировать решение. |
|
|
ОРГАНИЧЕСКАЯ ХИМИЯ — Тематические тексты
Главная → ОРГАНИЧЕСКАЯ ХИМИЯ — Тематические текстыТекст 1
Органическая химия — это изучение соединений, содержащих углерод.Его называют «органическим», потому что раньше ученые считали, что эти соединения обнаружены только в живых существах или окаменелостях. Однако в настоящее время в лабораториях и на фабриках можно искусственно производить огромное количество различных углеродсодержащих соединений для использования в промышленности. Например, лекарства, пластмассы и пестициды — все это синтетические органические вещества. Около 4. 5 миллионов из 5 миллионов известных сегодня соединений содержат углерод.
Текст 2
Углерод, важный неметаллический элемент, встречается в природе в трех формах или аллотропах.Есть графит, алмаз и бакминстер-фуллерен. Углерод может образовывать миллионы различных соединений (комбинаций элементов). Это связано с тем, что атом углерода может связываться с четырьмя атомами (углерода или других элементов) и потому, что атомы углерода могут соединяться в цепочки и кольца разных размеров и форм.
Текст 3 (96)
Органические (углеродсодержащие) соединения можно разделить на две основные группы — алифатические и ароматические соединения — в зависимости от способа связи атомов углерода.В алифатических соединениях атомы углерода связаны в цепочки. Эти цепочки могут содержать от двух до многих тысяч атомов углерода, при этом к каждому атому углерода присоединены другие типы атомов. В ароматических соединениях атомы углерода объединены в кольцо.
Текст 4 (94)
Кислоты — это вещества, выделяющие в воду ионы водорода. Щелочи — это вещества, выделяющие в воду ионы гидроксида (ионы, состоящие из водорода и кислорода). Если смешивать кислоты и щелочи, два типа ионов нейтрализуют друг друга, и образуется новое вещество, называемое химической солью.Кислотность или щелочность вещества можно измерить с помощью шкалы pH (потенциала водорода), которая изменяется от 1 до 14. Все кислоты имеют pH ниже 7; чем сильнее кислота, тем ниже pH. Все щелочи имеют pH больше 7; чем сильнее щелочь, тем выше ph. Нейтральные вещества, такие как вода, не являются ни кислотными, ни щелочными. У них pH 7.
Текст 5 (93)
Земля дает нам все необходимое сырье. Проблема в том, чтобы отделить вещества, которые мы хотим, от смесей, в которых они существуют естественным образом.Химики используют множество различных методов разделения в зависимости от типа смеси и свойств содержащихся в ней веществ. Иногда нам нужно разделить вещества и дома. Например, в кофеварке фильтр отделяет молотые кофейные зерна от жидкого кофе. Это называется фильтрацией.
Текст 6 (47)
Разделение различных частей соединения с помощью электричества называется электролизом. Чтобы это работало, соединение должно быть либо в расплавленном виде, либо растворенным в воде, и оно должно содержать ионы.Две электропроводящие пластины (называемые электродами) помещаются в разделяемое соединение (называемое электролитом). Когда пластины подключаются к батарее, через соединение проходит электрический ток, который постепенно разделяется на две части. Это происходит потому, что отрицательный электрод (катод) имеет избыток отрицательно заряженных частиц, поэтому он притягивает положительные ионы соединения. Положительный электрод (анод) притягивает отрицательные ионы.
Текст 7 (97)
При превращении веществ в новые вещества происходит химическая реакция.Чтобы это произошло, связи между атомами и молекулами должны разорваться и переформироваться по-разному. Поскольку связи могут быть прочными, для начала реакции часто требуется энергия, обычно в виде тепла. Новые вещества (продукты) имеют свойства, отличные от свойств исходных веществ (реагентов). Химические реакции происходят не только в лабораториях; они случаются повсюду вокруг нас — например, когда ржавеют машины или когда готовится еда.
Текст 8 (103)
Раствор образуется, когда одно вещество (обычно твердое) растворяется в другом (обычно в жидкости).Твердое вещество (называемое растворенным веществом) распадается на крошечные частицы и распространяется по жидкости (растворителю), так что твердое вещество больше не видно. Решения всегда ясны; если смесь мутная, это суспензия. Твердые частицы распространяются по жидкости, но частицы больше, чем у раствора. Если оставить суспензию отстояться, большая часть твердых частиц в конечном итоге утонет. Раствор таким образом не отделится.
